8 Ciri-Ciri Ion dan Contoh Ion Di Kehidupan Sehari-Hari
Ciri-Ciri Ion pada makhluk hidup memerlukan cairan untuk kelangsungan hidupnya, dimana setiap makhluk hidup memiliki kebutuhan cairan yang berbeda. Cairan dapat kita temukan di dalam berbagai buah-buahan yang banyak mengandung air. Saat kita melakukan aktivitas, tubuh akan mengeluarkan keringat yang mengakibatkan asupan cairan di dalam tubuh berkurang. Untuk mengembalikan cairan tubuh yang hilang dianjurkan mengkonsumsi cairan yang mengandung ion.
Baca Juga :
Ciri-Ciri Ion
Ion merupakan suatu ikatan yang terdapat pada atom dan mempunyai muatan yang besarnya sama akan tetapi memiliki tanda muatan yang berlawanan. Unsur yang dapat membentuk ikatan ion hanya dapat terjadi jika unsur-unsur yang direaksikan mempunyai perbedaan daya tarik elektron (keelekronegatifan) yang lumayan besar. Perbedaan tersebut memungkinkan adanya serah terima elektron. Adanya gaya tarik menarik antara ion positif dan ion negatif inilah yang disebut ikatan ion. Ion memiliki ciri-ciri secara khusus. Berikut penjelasan mengenai Ciri-Ciri Ion secara khusus. Baca juga : Hormon Giberelin)
1. Terdiri dari atom Logam dan Non Logam
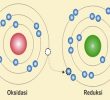
Unsur logam yaitu unsur yang kehilangan atau melepas elektron sedangkan non logam yaitu unsur yang mendapat atau menerima elektron. Contohnya seperti natrium merupakan unsur logam yang mudah melepas elektron sedangkan klorin merupakan unsur non logam yang mempunyai afinitas atau keelktronegatifan yang besar.Ketika natrium direaksikan dengan klorin, maka atom klorin akan menarik satu elektron dari natrium. Atom natrium berubah menjadi ion positif sedangkan atom klorin berubah menjadi ion negatif. Sehingga, ion-ion tersebut terjadi adanya gaya tarik menarik karena memiliki muatan yang berbeda dan membentuk NaCl.
Yang termasuk unsur logam antara lain Besi (Fe), Alumunium (Al), Perak (Ag), Emas (Au), Natrium (Na), Magnesium (Mg), Lithium (Li), dan yang terakhir yaitu logam dari golongan IA serta IIA. Sedangkan unsur yang termasuk kedalam unsur non logam antara lain Karbon (C), Hidrogen (H), Oksigen (O), Nitrogen (N), Phosfor (P), dan unsurdari golongan VVA, VI A serta VIIA. (Baca juga : Organ-organ pada Tumbuhan )
2. Terbentuk dari ion positif dan ion negatif
Karakteristik yang unik dalam ion yaitu terbentuk dari dua ion yaitu ion yang bermuatan positif dan ion yang bermuatan negatif. Tanpa adanya ion yang berlawanan muatan maka akan menyebabkan tidak adanya gaya tarik menarik antar ion . Sifat ion sendiri yaitu terdiri dari 2 jenis ion yang memiliki muatan positif dan negatif. (Baca juga : Jaringan Penyusun Daun Dikotil )
3. Terjadi serah terima elektron
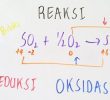
Ikatan kimia yang melibatkan elektron valensi salah satunya yaitu ikatan ion dimana adanya serah terima elektron dan melibatkan unsur elektro positif (logam) dan unsur elektro negatif ( non logam) .Reaksi serah terima pada oktet ditentukan dengan rumus kimia senyawa ion yang sesuai dengan aturan oktet, pada NaCl atom natrium akan melepas satu elektron , sedangkan atom klorin akan menyerap satu elektron. Jadi, setiap 1 atom klorin membutuhkan 1 atom natrium. Akan tetapi, bukan berarti bahwa satu ion Na hanya terikat pada sati ion Cl saja. (Baca juga : Faktor Internal Pertumbuhan )
4. Senyawanya berbentuk Kristal
Salah satu karakteristik ion yang khusus yaitu memiliki senyawa yang berbentuk kristal. Contohnya pada NaCl , dalam kristal NaCl setiap ion Na dikelilingi oleh 6 ion Cl dan setiap ion Cl dikelilingi 6 ion Na dalam suatu struksurtiga dimensi berbentuk kubus. (Baca juga : Penurunan Titik Beku )
5. Didalam larutan terurai menjadi ion positif (kation) dan ion negatif (anion)
Saat kedua unsur ion di masukkan ke dalam larutan maka akan terurai menjadi ion negatif dan ion positif , dimana nantinya akan menimbulkan daya tarik menarik.logam atau ion positif memiliki daya tarik yang lemah sedangkan pada ion negatif atau non logam memiliki daya tarik yang sangat besar. (Baca juga : Gangguan pada Sistem Pernapasan )
6. Dapat menghantarkan arus listrik
Ion memiliki ciri khas yang unik yaitu dapat menghantarkan aliran listrik .Karena ion merupakan larutan elektrolit , dimana larutan elektrolit memiliki daya hantar untuk mengalirkan arus listrik . Contoh ion yang dapat menghantarkan arus listrik yaitu NaCl. (Baca juga : Faktor Eksternal Pertumbuhan )
7. Titik didih Tinggi
Senyawa ion mampu mendidih diatas 900 derajat celsius sedangkan pada senyawa kovalen hanya mendidih di bawah 200 derajat celcius , dapat disimpulkan bahwa senyawa ion memiliki titik didih yang tinggi.Pada suhu kamar semua senyawa ion berubah menjadi zat padat, keras akan tetapi rapuh. (Baca juga : Penurunan Tekanan Uap )
8. Larut dalam air
Senyawa ion cenderung larutdalam air , akan tetapi tidak larut ke dalam larutan pelarut organi misalnya aseton, patreloum eter, alkohol dan trikloroetana). Contohnya saja pada garam dapur , dia larut dalam air akan tetapi tidak larut dalam kloroform. (Baca juga : Organ-Organ Pernapasan )
Penjelasan diatas merupaka karakteristik yang harus dimiliki senyawa ion . Untuk membentuk senyawa ion terdapat syarat dan ketentuan yang harus dimiliki suatu unsur. Berikut mengenai syarat terjadinya ikatan ion.
Syarat Terjadinya Ikatan Ion
- Ikatan ion harus terjadi antara atom logam yang akan membentuk ion positif dengan atom non logam yang akan membentuk ion negatif, hal ini dikarenakan agar timbul gaya tarik menarik dan serah terima elektron. (Baca juga : Molalitas )
- Ikatan ion terjadi antara atom-atom yang mempunyai suatu energi ionisasi rendah dengan atom-atom yang mempunyai afinitas elektron yang tinggi. Hal ini dapat dikatakan bahwa ikatan ion akan terjadi apabila antara atom-atom dengan keelektronegatifan tinggi. (Baca juga : Contoh Elektrolit Lemah )
Contoh Ion Di Kehidupan Sehari-Hari
1. NaCl
Senyawa Na Cl tersusun dari unsur Na dan Cl yang merupakan salah satu contoh ion yang setiap hari kita temui. NaCl atau garam dapur sudah tidak asing bagi kita , khususnya bagi ibu rumah tangga. Senyawa NaVl memiliki karakteristik dari Na merupakan unsur logam dan Cl merupakan unsur non logam. Satu elektron dari Na akan ditarik oleh unsur Klorida sehingga akan menimbulkan gaya tarik menarik antara Na dan Cl yang membentuk NaCl. Senyawa ini juga merupakan contoh bahwa dalam proses reaksi kimia, banyak kemungkinan yang dapat terjadi. Natrium dan Klorida merupakan dua unsur yang sangat beracun dan berbahaya , ketika bergabung menjadi senyawa yang sangat bermanfaat , dan bahkan dibutuhkan oleh manusia dalam kehidupan sehari-hari. (Baca juga : Kenaikan Titik Didih )
2. CaCl2
CaCl2 atau Kalsium Klorida ini tersusun dari Ca (kalsium) merupakan unsur logam dan 2 atom Cl (Klorida) yang merupakan unsur nob logam. Biasanya Kalsium Klorida (CaCl2) ini digunakan pada kolam renang , yang biasanya disebut dengan kaporit . Kegunaan Kalsium Klorida yang dimasukkan ke dalam kolam renang aitu agar tidak bersifat korosif dan tidak merusak struktur logam pada kolam. (Baca juga : Perbedaan Larutan Elektrolit dan Non Elektrolit )
3. NaF
NaF merupakan senyawa yang terbentuk dari 2 unsur yaitu Natrium (Na) serta Flor (F). Unsur Na merupakan unsur logam sedangkan unsur F merupakan unsur non logam. Natrium Florida ini biasanya digunakan pada pasta gigi yang berfungsi untuk memutihkan gigi dan menguatkan struktur gigi. (Baca Juga : Gangguan Pada Sistem Pernapasan)
Penjelasan diatas merupakan Ciri-Ciri Ion secara umum . Didalam ion mempunyai keuntungan yang sangat bermanfaat bagi kehidupan sehari-hari seperti yang sudah dijelaskan diatas antara lain bisa digunakan sebagai garam dapur, kaporit serta untuk memutihkan gigi.